由于医疗器械是救死扶伤、防病治病的特殊产品,其在国际上不仅只是一般的上市商品在商业环境中运行,它还要受到国家和地区法律、法规的监督管理,如美国的fda、欧盟的mdd(欧盟医疗器械指令)、中国的《医疗器械监督管理条例》。因此,医疗器械仅按iso 9000标准的通用要求来规范是不够的。其适用标准必须受法律约束,在法规环境下运行,同时必须充分考虑医疗器械产品的风险,要求在医疗器械产品实现全过程中进行风险管理。为此iso组织颁布了iso 13485标准(国家食品药品监督管理总局等同转换为yy/t0287标准),对医疗器械生产企业的质量管理体系提出了专用要求,为医疗器械的质量达到安全有效起到了很好的促进作用。
iso 13485标准的全称是《医疗器械质量管理体系 用于法规的要求》(medical device-quality management system-requirements for regulatory)。该标准由sca/tc221医疗器械质量管理和通用要求标准化技术委员会制定,是以iso 9001为基础的独立标准,是适用于法规环境下的管理标准:从名称上即明确是用于法规的质量管理体系要求。所以除了专用要求外,可以说iso 13485标准实际上是医疗器械法规环境下的iso 9001。标准规定了对相关组织的质量管理体系要求,但并不是iso 9001标准在医疗器械行业中的实施指南。
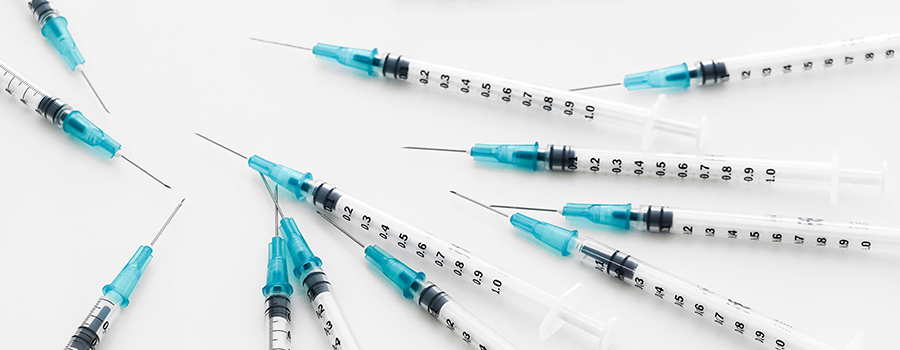
iso 13485标准适用于履行国际、欧洲和本国的法律法规要求的医疗产品开发、制造和销售医疗设备的企业,想要在国际、欧洲和本国市场上展示其竞争和绩效能力的企业,以及希望按此标准实施文件化管理体系的企业。供应商和其他在增值链内的服务提供商必须确保其产品与顾客的要求相一致。
noa|挪亚在国内拥有资深的iso 13485审核员队伍,充足的审核资源可以及时为客户提供本土化、专业化的iso 13485认证服务,可帮助客户提高保证产品质量的水平,有利于增强企业竞争力,消除国际贸易中的技术壁垒。
○ iso 13485:2016《医疗器械质量管理体系 用于法规的要求》
○ gb/t 42061-2022/iso 13485:2016《医疗器械 质量管理体系 用于法规的要求》
○ 提高和改善企业的管理水平,规避法律风险,增加企业的知名度;
○ 提高和保证产品的质量水平,使企业获取更大的经济效益;
○ 有利于消除贸易壁垒,取得进入国际市场的通行证;
○ 有利于增强产品的竞争力,提高产品的市场占有率;
○ 通过有效的风险管理,有效降低产品出现质量事故或不良事件的风险。